PFOについてはこちらも参照
特に専門は絞っていない内科医のブログ *医学情報のブログです. 個別の相談には応じられません. 現在コメントの返事がうまくかけませんのでコメントを閉じています. コメントがあればFBページでお願いします
ページ
2021年12月23日木曜日
PFOにおける塞栓症リスクと閉鎖療法のベネフィット
2021年12月20日月曜日
抗セントロメア抗体の値と強皮症の進行リスク
抗セントロメア抗体は限局型全身性強皮症の抗体として有名.
他にも原発性胆汁性胆管炎などでも陽性となる.
抗セントロメア抗体の抗体価と予後への影響を評価した報告
(Arthritis & Rheumatology Vol. 73, No. 12, December 2021, pp 2338–2347)
・5つのCohortより, IgG ACA陽性でVery early SScを満たす, またはSScのACR/EULAR013基準を満たす患者を評価.
・Very early SScは, IgG ACA陽性で以下の1つ以上を満たし, さらにACR/EULAR2013のSSc基準を満たさない患者で定義;
Raynaud現象, Puffy fingers, NFC異常
・BaselineのIgG ACAの値と, その後のSScへの進展リスク, 臓器障害リスクを評価した.
・臓器障害はDigital ulcer, ILD, 心筋障害(不整脈や伝導障害, EFの低下, 心外膜炎など), 肺高血圧, 消化管障害を含む
・ACAの評価はFEIA(酵素免疫測定法)を用いて測定
IgG ACAのカットオフは 7 U/mL(製品より)
IgMとIgAも測定. 健常人サンプルよりカットオフはIgA ACA 37AU/mL, IgM ACAは13AU/mLとした.
アウトカム
・IgG ACA陽性例 625例のうち,
Very early SScが138例, 臓器障害(-)のSScが240例, 臓器障害(+)のSScが247例
・IgG ACAはVery early SScで274[93-662] U/mL臓器障害(-)SScで480[197-990]
臓器障害(+)SScで619[263-1077] とSSc症例や臓器障害(+)例で高くなる傾向がある
・Very early SScとSScを比較すると, 有意にACA値がSScで高値.
・さらに, Very early SScにおいて, IgG ACA値が高いと, SScへ進行するリスクも高くなる.
Very early SSc 115例のうち, 5年間のフォローにてSScへ進行する例は48例(42%)認められた.
母集団におけるACA値の分布
Very early SScにおける, ACA値とその後のSSc進行例と非進行例
2021年12月16日木曜日
ワクチン投与時のDMARDs 薬剤調節
メモがてら:
Impact of disease-modifying antirheumatic drugs on vaccine immunogenicity in patients with inflammatory rheumatic and musculoskeletal diseases
Ann Rheum Dis 2021;80:1255–1265.
DMARDsのワクチンへの影響は以下の通り:
・MTX, ABA, RTXはワクチンへの影響が顕著.
これを踏まえた, 各種ワクチン接種時の投薬調節推奨
ワクチン | ワクチンの推奨 | DMARDの調節 |
インフルエンザ | 全患者に毎年4価ワクチンを推奨 | RTX: RTX開始前に投与. 最終投与から6ヶ月以上開けて, 次回投与の4wk以上前に投与する |
肺炎球菌 | 免疫抑制状態の患者全例で推奨 | RTX: RTX開始前に投与. 最終投与から6ヶ月以上開けて, 次回投与の4wk以上前に投与する |
帯状疱疹 | 50歳以上で推奨 | RTX: RTX開始前に投与. 最終投与から6ヶ月以上開けて, 次回投与の4wk以上前に投与する |
HBV | HBV感染リスクがある人で推奨 | RTX: RTX開始前に投与. 最終投与から6ヶ月以上開けて, 次回投与の4wk以上前に投与する |
HPV | 一般的なガイドラインに準拠(各国) | RTX: RTX開始前に投与. 最終投与から6ヶ月以上開けて, 次回投与の4wk以上前に投与する |
破傷風 | 一般的なガイドラインに準拠(各国) | RTX: RTX開始前に投与. |
Yellow Fever | 免疫抑制患者では避ける | 禁忌 |
ワクチン | ワクチンの推奨 | DMARDの調節 |
SARS-CoV-2 | 全ての人で推奨される | RTX: 最終投与からなるべく空けて投与. 次回投与から2-4wk前に投与する. MTX: mRNAワクチン後1週間休薬. 単回投与ワクチンでは2週間休薬する. MMF, JAK阻害薬: ワクチン後1週間休薬 以下は投与調節不要 |
2021年12月8日水曜日
黄色ブドウ球菌菌血症におけるPET/CT
黄色ブドウ球菌菌血症(SAB)におけるPET/CTの意義を評価したProspectiveのCase-control study.
(Clinical Infectious Diseases® 2021;73(11):e3859–66)
私個人としては, SABにおいて, 感染のFocusがどこなのか, それが臨床判断とどの程度解離しているのかが気になり, 読んでみることにした.
成人のSAB症例を対象とした前向きCohort.
・SAB診断の7-14日後にFDG-PET/CTを評価した症例(2015-2019年)をIntervention groupとし,
FDG-PET/CTが行われなかったSAB症例(2015-2018年)をControl groupとした.
・PET/CT検査を施行するかどうかはは臨床医の判断により行われた.
・Control groupは, 以下の条件をMatchさせている;
1) SAB診断〜Intervention群におけるFGD-PET/CT撮影までの期間, 生存していた患者
2) MSSA, MRSAによる菌血症
3) インフォームドコンセントが得られている
4) Charlson’s comorbidityスコア(±3まで許容されるが, best matchを選択)
5) 年齢(±10歳までは許容されるが, best matchを選択)
第7病日まで生存していたSAB症例が531例.
・このうちPET/CTが施行されたのが149例(151エピソード)
Control群として150例(151エピソード)を選択し, PET/CTによる予後への影響を評価.
両群の母集団
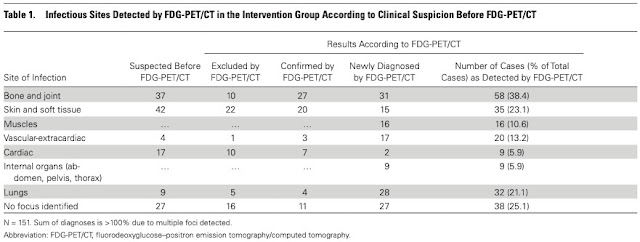
PET/CTによる診断への影響
・感染のFocusで最も多かった部位が骨関節.
臨床上疑われたのが37例, PET/CTで否定されたのが10例, 新たに診断されたのが31例
・多くが臨床判断とPET/CTの集積に解離がある.
90日死亡に関連する因子.
・年齢や合併症, 院内感染 治療開始後3日を超えての発熱や菌血症は 有意に死亡リスクを上昇させる因子
・PET/CTの施行は死亡リスクの低下に関連
--------------------------
SABにおいて, 臨床判断の感染Focusのおよそ1/3~1/2, または半分以上がPET/CTで評価すると他のFocusであった.
皮膚軟部組織, 心内膜炎は高く見積もりがち: IEは心配だし, SAは軟部組織からが多いしそれはしかたない.
一方で, 肺や骨関節, 筋, 血管(心臓以外)は低く見積がちな傾向がある.
2021年12月7日火曜日
帯状疱疹ワクチンによるギランバレー症候群のリスク
(JAMA Intern Med. 2021;181(12):1623-1630. doi:10.1001/jamainternmed.2021.6227)
VZVワクチンによるGBSリスク
・65歳以上でRecombinant VZVワクチン(RZV, シングリックス)を接種した849397例と 65歳以上で生ワクチン(Zostavax, ZVL)を接種した1817099例において, ワクチン接種後(1-42日)におけるGBS発症リスクを評価した報告
・6ヶ月以内にGBSの診断が既にされている患者や, RZVを添付文章外使用した患者(3回以上投与した患者, 1回目投与から42日以内に2回目を投与した患者)は除外.
・RZVにおけるGBSリスクを評価するために,
ZVL投与後1-42日で発症したGBSをControlとして評価.
また, Self-controlとして, Control periodとしてワクチン接種後 43日~183日を設定(1回目, 2回目ともに). その間に発症したGBSをControlとしてRZV投与後1-42日におけるGBS発症率を比較した.
両群の母集団
アウトカム
・GBS発症症例
RZVとZVLにおける比較
・GBSはRZVで15例(100万件で0.29例), ZVLで9例(100万件で0.12例)
RZVはZVLと比較して有意にGBSリスクが高い(RR 2.34[1.01-5.41])
RZVのSelf-controlにおける評価
・Self-controlでは, RR 4.30[1.76-10.53]
100万件のワクチン接種あたり, 6.47[2.50-10.45]例のGBSが増加
Discussionより
・VZV再活性化後のGBSリスクはRR 4.0[1.9-8.7]
100万回の感染エピソードあたり12.8例[3.7-31.9]と推測される
・このデータとワクチンの効果(97%)を考慮すると, 100万人の完全接種者あたり6.26件のGBSが発症する.
・RZVのリスクベネフィットを調査したモデルによると,
60-69歳におけるRZVワクチン接種において,
過剰なGBSは6.3例,
予防できたVZV再活性化は61600例
(このうち死亡の可能性62例, 眼合併症5500例, 帯状疱疹後神経痛が9350例) とRZVのVZV再活性化予防効果はGBSリスクを上回るベネフィットと捉えられる.
膠原病に伴う血球貪食症候群の背景疾患
膠原病に伴うHLHの背景疾患を文献Reviewにて調査した報告
(Eur Rev Med Pharmacol Sci. 2012 Oct;16(10):1414-24.)
・117論文, 421例
疾患 | 頻度 |
SLE | 94例 |
AOSD | 37例 |
RA | 13例 |
JRA | 219例 |
DM | 7例 |
川崎病 | 25例 |
SSc | 5例 |
ベーチェット病 | 1例 |
PAN | 6例 |
AS | 2例 |
MCTD | 1例 |
サルコイドーシス | 5例 |
pSS | 3例 |
GPA | 1例 |
分類不能 | 2例 |
・背景疾患として多く報告されているのはJRA(小児リウマチ), SLE, AOSD, 川崎病.
・活動性感染症の合併も含まれる : CMV(4例), EBV(4例), HSV-1, パルボB19, 粟粒結核, Histoplasmosis, leishmaniasis
SLEの5/94, RAの1/13, AOSDの2/37で感染の併発があった.
・免疫抑制療法がTriggerとなった 症例も20例あり.
原因薬剤はADA, IFX, ETN, レフルノミド, サルファサラジン, AZA, MTX
・他に非ホジキンリンパ腫や抗マラリア薬が誘因となった症例もあり
SLEにおけるHLH発症の誘因として, 多いものはフレアと感染症の合併.
(Cureus 13(10): e18822. DOI 10.7759/cureus.18822)
・感染症ではEBVが最も多い誘発因子であり, ついでCMVが多い.
・細菌感染症も誘因となり得る
・ヒドロキシクロロキンはHLHリスクを低下させる
SLEとAOSDに伴うHLHを比較した報告では,
(ARTHRITIS & RHEUMATOLOGY Vol. 66, No. 8, August 2014, pp 2297–2307)
・SLEを背景とする場合はよりWBCが低値, CPRが低い.・AOSDではWBC減少は生じにくく, フェリチンが数万と著明に高値となる
--------------------------
あまりデータがない分野
2021年12月1日水曜日
リツキシマブ使用患者におけるPCPの予防
PCPはCD4+ cellの活性低下がリスクとなるが, 動物実験ではB cellも免疫に関与している結果がでている.
・Mayo clinicにおいて, 1998-2011年に リツキシマブ使用中に発症したPCP症例は30例.
ステロイド併用が73%で, 10%はリツキシマブ単独投与下でのPCP発症であった.
PCPの予防投与をされていたのは1例のみで, 大半が予防投与無し.
53%がICU管理となり, 死亡率は30%であった.
(Chest 2013;144:258-265)
リツキシマブ使用中の患者でのPCPの予防推奨は未だはっきりしていないのが現状.
そんななか, 韓国より後ろ向き解析が発表.
(Chest 10.1016/j.chest.2021.11.007)
RTX使用患におけるPCP予防の効果を調査した韓国からの報告
・韓国のSeoul National Univ. Hosp. において, 2002-2018年にRTXが使用された患者群 3524例を解析.
・このうち血液疾患が2500例, リウマチ性疾患が559例, 臓器移植が465例.
・ST合剤によるPCP予防が行われたのが1001例であった (RTX投与開始から28日以内に開始された群をITT解析で採用. 28日を超えて開始された例が254例あり. )
・アウトカムは予防の有無と1年間におけるPCP発症リスク.
・PCPの診断は検体からの病原菌の検出(染色やPCR)があった症例で, さらにエキスパート2名がカルテをReviewし, 経過や画像より妥当性を検討.
母集団
a) PN, ASP, クリオグロブリン血管炎を含むb) ITP, TTP, IVL, WMを含む
c) GFR<60mL/min, d) Ly<800/µL, e) PSL≥30mg/d
・膠原病ではAAVとRAが多い 他はSLE, 炎症性筋疾患
・AAVでは予防されている例が多いが, RAでは少ない
・ST合剤の投与期間は 平均153.8±107.6日間
アウトカム
・2759.9pt-yのフォロー期間でPCPは92例で発症.
(リウマチ性疾患10例, 血液疾患74例, 移植18例)
・疾患群別の発症率(/100pt-y, Control群)は,
全体で4.11[3.26-5.12]
リウマチ性疾患で2.96[1.19-6.09],
血液疾患 4.50[3.44-5.78],
臓器移植 7.01[3.63-12.25]
・RTX開始〜PCP発症までの中央期間は86±80日間
・ PCP関連死亡率は27.2%
・PCPの発症リスクに大きく関与する因子は,
腎機能低下(GFR<60) aSHR 2.38[1.75-3.23]
高用量ステロイド(PSL≥30/d) aSHR 3.09[2.22-4.30] であった.
ST合剤による予防効果
・PCPの頻度は Control群で4.13, 予防群で1.47/100pt-yと 有意に予防群で低下
・高用量GC使用例を除外した群では aSHR 0.14[0.04-0.52]
IPTWを適応しない場合 aSHR 0.26[0.14-0.47]
1:1のPropensity score matchedでの比較 aSHR 0.35[0.16-0.79]
・他の免疫抑制療法/抗癌剤を使用していない群でも同様の予防効果
・予防によるNNTは32[24.8-39.4]
副作用によるNNHは101[61.9-261.1]
・また, 予防効果は140日以上継続した症例でさらに高い.
疾患群別の評価では
・リウマチ性疾患, 血液疾患, 移植患者群すべてST投与による PCP予防効果は良好に得られる.
・リウマチ性疾患患者では, 死亡リスクの低下効果もあり.
・疾患群別のNNTは,
リウマチ性疾患 23[16.6-36.4]
血液疾患 36[27.7-46.6],
移植患者では27[13.6-101.1]
・高用量GC併用群では17[12.1-25.7]とさらにNNTは良好となる
---------------------------
RTX使用患者でもST合剤によるPCP予防は考慮する価値がありそう
国内ではAAVが主なので, 大体併用していますが