昨今Iphoneに接続するECGデバイスや、Apple watchによるECG測定など, 色々簡易なECGデバイスが出てきている.
これらデバイスを使用すれば, 一般市民でも不整脈のスクリーニングが可能であるが, それが実際どの程度の予後を改善させる効果があるのだろうか?
STROKESTOP: スウェーデンのHallandとStockholmにおけるRCT.
(Lancet 2021; 398: 1498–506)
・75-76歳の住民を対象とし, Afのスクリーニング(14日間の間欠的ECG評価)を行う群とControl群に割り付け, 臨床アウトカムを比較した.
・除外基準は無し
・スクリーニング群において, 実際スクリーニングに参加し, Afが認められれば抗凝固療法を開始.
・スクリーニングは初回ECGを評価し, Afが認められない群では14日間, 1日2回のECG評価を行う(Single lead ECG).
・最低5年間以上フォローし, 両群におけるStrokeリスク, 出血リスクを比較した.
スクリーニング群は13979例 このうち7165例(51.3%)が 実際にスクリーニングに応じた.
・スクリーニング群に割り付けられたが, 応じなかった “Non-paticipants”は, より併存症や内服, 好ましくない社会因子が多い.
アウトカム
・最初の1年間でAfと診断された患者は
スクリーニング群で12.1%→15.1%(+3%)
Control群では12.8%→14.1%(+1.3%)
・しかしながら両群で抗凝固療法を行った症例数に差は認めない(スクリーニング群で1年以内に増加するような曲線は認められている)
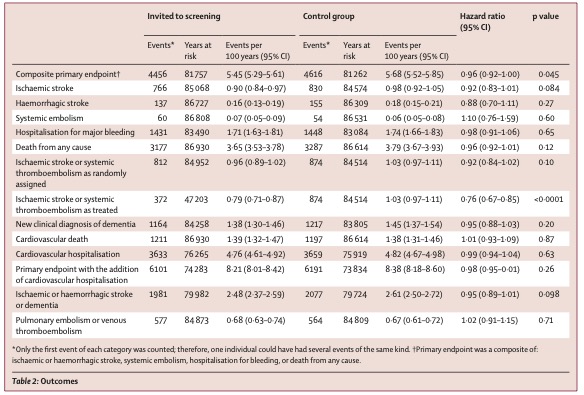
・スクリーニングを行う群ではStroke, 血栓症, 出血入院, 死亡の複合アウトカムの改善が認められたが, その差は少ない
・個々のアウトカムでは有意差なし.
・実際スクリーニングに参加した人と不参加(non-paticipants), Control群を比較すると, その差は大きくなる
これは, 住民全体を対象とし, 臨床アウトカムを評価した重要な論文である
他にもAf検出率を評価したスクリーニングの文献はいくつかある;
他のAfスクリーニングのStudy
STROKESTOP II: ストックホルム在住の75-76歳の住民をスクリーニング群とControl群に割り付け.
(Europace (2020) 22, 24–32)
・スクリーニング群ではNT-proBNPを評価し, <125ng/Lを低リスク群, ≥125ng/Lを高リスク群とした
低リスク群では1回のSingle-lead ECGを評価
高リスク群では1日4回のSingle-lead ECG評価を14日間継続
Single-lead ECGはHand-held deviceで1回30秒評価
・Afが認められれば循環器内科紹介. また以下があれば紹介する;
NT-proBNP ≥900ng/Lで心不全の既往がない患者
Afがすでに知られており, 抗凝固療法がされていない患者
アウトカム
・新規Afは全体で2.6%[2.2-3.0]で検出.
高リスク群では4.4%[3.7-5.1]
・初回ECGにおけるAfの検出をアウトカムとした時の NT-proBNP値の感度/特異度
NT-proBNPとAf
・2週間のフォローでAfを検出した症例では, NT-proBNPの中央値は305[199-522].
・NT-proBNPが高いほど, Afが診断される可能性も高い
・NT-proBNP値とCHA2DS2-VAScによるAf検出率
NT-proBNPが>353ng/Lの例では検出率がかなり上昇する
mSToPS: 米国の大手健康保険の加入者を対象としたRCT
(JAMA. 2018;320(2):146-155. doi:10.1001/jama.2018.8102)
・モニタリング参加希望者は, ランダムに即時開始群と4ヶ月後に開始群に割り付け, その4ヶ月間の間にどの程度Afが多く検出されるかを評価.
・対象患者は75歳以上の高齢者, または男性は55歳以上, 女性は65歳以上で1つ以上の併存疾患を有する患者.
すでにAfの診断がされている患者は除外
・Afスクリーニングは装着型のECGモニタリングを2週間着用し, 3ヶ月あけて再度チェックする.
アウトカム
・早期スクリーニング群で最初の4ヶ月に検出されたAfは3.9%
晩期群では0.9%であり, 3.0%[1.8-4.1]がスクリーニングで多く検出された
REHEARSE-AF: AliveCor Kardiaを用いたモニタリング
(Circulation. 2017;136:1784–1794.)
・Ipad, Iphoneに接続して使用するECGデバイス.
・65歳以上でCHADS-VASc ≥2を満たす, Af(-)患者を対象とし, このデバイスを使用して週2回測定, 12ヶ月継続(+症状がある時測定)群とControl群に割り付け, Af検出率を比較.
・スクリーニング群での計測頻度
アウトカム
・12ヶ月において, Afが検出されたのは
スクリーニング群で19例(3.8%) vs Controlで5例(1.0%) HR 3.9[1.4-10.4]
・Afが検出された群とされなかった群で, モニタリングのアドヒアランスに差は認めず
・Af診断のリスク因子
高齢者, 動脈疾患, CHADS-VAScスコアがリスクとなる.
・12ヶ月における血栓症やStrokeリスクは有意差なし
-----------------------------
高齢者における簡易デバイスを用いたAfスクリーニングは, Strokeや血栓症などの複合アウトカムリスクを低下させる可能性がある.
大体, 高齢者やリスク(+)群において簡易デバイスを用いてAfスクリーニングを行うと, およそ2-3%多く新規Afが検出されることになる.