ふと気になり最新のReviewをチェック.
コクランより2018年にCVカテーテルのフラッシュに関してMetaがありました.
CVカテーテルにおけるフラッシュ
ヘパリン vs NSフラッシュを比較したMeta(Cochrane)
(Cochrane Database of Systematic Reviews 2018, Issue 7. Art. No.: CD008462.DOI: 10.1002/14651858.CD008462.pub3.)
・CVCのフラッシュとしてヘパリンを用いる群とNSを用いる群で比較した11 RCTsのMeta(N=2392)
・ヘパリンの濃度は様々で10-5000IU/mL
アウトカム;
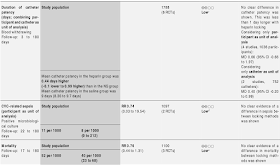
・閉塞リスクはヘパリン群で有意に低い: RR 0.70[0.51-0.95]
ただし, NNTBは42[32-250], Quality of the EvidenceはVery low.
・CVCの開存期間は有意差なし: MD 0.44d[-0.10~0.99]
CVC関連敗血症 RR 0.74[0.03-19.54]
死亡リスク RR 0.76[0.44-1.31]
出血リスク RR 1.32[0.57-3.07]
HITリスク RR 0.21[0.01-4.27]
2017年のMeta-analysisでは,
・ヘパリンフラッシュは<30日の短期留置群において, 有意な開存維持効果が得られる: RR 1.52[1.02-2.27]
・全体の評価, >30日の長期留置群では有意差は認めない.
・HITリスク上昇も無し
(Critical Care (2017) 21:5)
A-lineにおけるフラッシュ
1951-2012年に発表された10論文のReview.
(JVascAccess 2014;15(2): 123-127)
・ヘパリンの濃度は1-5U/mLと様々
フラッシュも間欠的〜持続様々
間欠的では8h毎が多い.
アウトカム
・48h以上の長期間のA-line開存率はヘパリン群で良好.
・ヘパリンフラッシュ群で, HITの報告は無し.
同じく2014年発表のCochraneでは,
ヘパリンフラッシュとNSを比較した7 RCTs(N=606例)を解析したところ
Studyの背景, 統計的な不均一があり, Metaができない結果であった.
Studyのまとめ
・これら報告の結果をみると,
両群で同等〜ややヘパリンで開存期間が延長する結果が多い.
とはいえその差は数時間〜1日程度.
----------------------------------
CVCやA-lineのフラッシュについてはヘパリンを用いたほうが, 長期的な閉塞リスクは低下する可能性がある. ただし, Evidenceレベルは低い点から, 必ずしもそうせねばならないわけではない.
実際論文の執筆者は, 「ルーチンのヘパリン使用を推奨しない」、と結論しているものがほとんど.
また, HIT(ヘパリン誘発性血小板減少症)はヘパリンフラッシュでも生じるよ, とよく言われているが, これら報告におけるHITの発症率は著しく低く, 両群で差はつかない.
症例報告レベルでは, ヘパリンフラッシュにより重度のHITを生じた報告もあるが, 非常に稀である, と認識しておいてもよいと思う.
特に専門は絞っていない内科医のブログ *医学情報のブログです. 個別の相談には応じられません. 現在コメントの返事がうまくかけませんのでコメントを閉じています. コメントがあればFBページでお願いします
ページ
▼
2019年5月31日金曜日
2019年5月28日火曜日
抗凝固療法, アスピリン使用患者におけるPPI: COMPASS trial
参考: 抗凝固療法使用患者におけるPPI併用の意義
COMPASS trialにおけるPPI使用症例の比較が発表されました.
COMPASS trial: 安定した動脈硬化性血管疾患の既往がある患者を対象とした3x2 partial factrial designのDB-RCT.
(N Engl J Med 2017;377:1319-30.)
・患者は冠動脈疾患もしくはPADの既往がある群.
20年以内にMI既往, 多枝病変, 狭心症既往がある患者
<65歳の冠動脈疾患患者では, さらに2つ以上のリスク因子を有する群(喫煙, DM, GFR<60mL/分, 心不全, 1ヶ月以上前の非ラクナ梗塞)
・除外項目: 出血リスクが高い, 最近のStroke, 出血性梗塞やラクナ梗塞, 重症心不全, GFR<15mL/分, DAPT, 抗凝固施行, 他の抗血小板療法, 心血管疾患以外で予後不良な状況
上記患者群を
・Rivaroxaban 2.5mg bid + ASA 100mg
vs Rivaroxaban 5mg bid単独
vs ASA 100mg単独群に割付け, 血管イベントリスクを評価.
さらに, 上記のうち, 臨床的にPPIが不要と判断された患者において
Pantoprazole 40mg vs Placebo群に割り付け上部消化管出血リスクを比較した.
Rivaroxaban, ASAの比較については省略.
結果としては, ASA単独と比較して, Rivaroxaban 2.5mg bid + ASA群において, 有意に脳梗塞リスクは低下し, 脳出血リスクは有意差なし. Rivaroxaban 5mg bidでは脳梗塞リスクは低下するが, 脳出血リスクは上昇する.
この結果により, Rivaroxaban, ASAの評価は途中でStudyは終了となっている
Pantoprazoleの比較は平均3年間継続
(Gastroenterology (2019), doi: https://doi.org/10.1053/j.gastro.2019.04.041.)
母集団
アウトカム
・PPI使用の有無で, 上部消化管出血リスクは同等
COMPASS trialにおけるPPI使用症例の比較が発表されました.
COMPASS trial: 安定した動脈硬化性血管疾患の既往がある患者を対象とした3x2 partial factrial designのDB-RCT.
(N Engl J Med 2017;377:1319-30.)
・患者は冠動脈疾患もしくはPADの既往がある群.
20年以内にMI既往, 多枝病変, 狭心症既往がある患者
<65歳の冠動脈疾患患者では, さらに2つ以上のリスク因子を有する群(喫煙, DM, GFR<60mL/分, 心不全, 1ヶ月以上前の非ラクナ梗塞)
・除外項目: 出血リスクが高い, 最近のStroke, 出血性梗塞やラクナ梗塞, 重症心不全, GFR<15mL/分, DAPT, 抗凝固施行, 他の抗血小板療法, 心血管疾患以外で予後不良な状況
上記患者群を
・Rivaroxaban 2.5mg bid + ASA 100mg
vs Rivaroxaban 5mg bid単独
vs ASA 100mg単独群に割付け, 血管イベントリスクを評価.
さらに, 上記のうち, 臨床的にPPIが不要と判断された患者において
Pantoprazole 40mg vs Placebo群に割り付け上部消化管出血リスクを比較した.
Rivaroxaban, ASAの比較については省略.
結果としては, ASA単独と比較して, Rivaroxaban 2.5mg bid + ASA群において, 有意に脳梗塞リスクは低下し, 脳出血リスクは有意差なし. Rivaroxaban 5mg bidでは脳梗塞リスクは低下するが, 脳出血リスクは上昇する.
この結果により, Rivaroxaban, ASAの評価は途中でStudyは終了となっている
Pantoprazoleの比較は平均3年間継続
(Gastroenterology (2019), doi: https://doi.org/10.1053/j.gastro.2019.04.041.)
母集団
アウトカム
・PPI使用の有無で, 上部消化管出血リスクは同等
・画像や検査で証明された上部消化管出血はPPI群で少ないものの, その差は0.2%程度.
NNTはおおよそ500と多い.
・抗凝固療法, ASA投与群別の評価.
ASA 100mg投与群でのみ有意差を認めるが, Absolute risk reductionは微々たるもの.
-----------------------------
DOAC(rivaroxaban)やASA使用患者におけるPPIの予防投与は,
明らかな上部消化管の病変からの出血リスクは軽減するが, NNTは500オーバーと実感するのは難しいレベル.
でのPPIによる上部消化管出血リスク軽減効果はNNT 200程度であり,
「DOACやASAを使用しているからPPI」ではなく,
さらに+αのリスク因子を考慮し, PPIの開始, 継続を検討する必要がある.
2019年5月24日金曜日
β-Dグルカンの偽陽性
β-Dグルカンは深在性真菌症やニューモシスチス肺炎の診断に有用な検査であるが, アルブミン投与やIg投与, 輸血, 透析, 抗真菌薬などで偽陽性となることが指摘されている.
実際どの程度これらの因子が影響するのか?
アルブミンとβ-Dグルカン
ICUでβ-DGを評価した267例の後ろ向き解析.
(Eur J Clin Microbiol Infect Dis. 2015 Feb;34(2):357-65. )
・BG試験におけるIFIに対する感度, 特異度を, アルブミン投与, Ig投与, 輸血施行群で評価, 比較
・全体の評価では, カットオフ 95.9pg/mLで, 感度82.9%, 特異度56.7%
・アゾール系抗真菌薬の使用, IVIG, RBC輸血はBG試験の感度, 特異度に影響は認められず.
・アルブミン投与のみ, BG試験の感度, 特異度に影響あり
>30gのAlb(20%製剤で>150mL)を2日以内に投与している場合, BG試験の感度は低下する. 感度36.2%[25.0-48.7], 特異度84.7%[77.5-90.3]
この場合のカットオフは203.7pg/mL
中国における前向きStudy: ICU患者267例において, Alb投与前後のβ-DGを評価.
(Zhonghua Wei Zhong Bing Ji Jiu Yi Xue. 2015 Aug;27(8):672-6. )
・β-DGの変化(ng/L)
IFI否定群では 11.25±2.33 → 10.99±1.07, p=0.085
IFI疑い群 53.14±5.53 → 49.22±8.11, p=0.693
IFI濃厚群 90.30±9.38 → 85.41±10.11, p=0.860
IFI群 100.98±19.24 → 103.21±17.66, p=0.449
アルブミン投与してもβ-Dグルカンの上昇に関連しない報告もあれば, 大量投与により偽陽性が増加する報告もある.
実際アルブミン製剤にどの程度β-Dグルカンが含まれているかを評価した報告もある.
人血清アルブミン5%製剤の国産製品3種類(A-C)と海外製品1種類(D)における含有量を評価
(Therapeutic Research 2013;34:1261-1269)
・β-Dグルカン(pg/mL)
・海外製品の含有量が高いが, 国産製品の含有量は多くはない.
・30pg/mLと仮定すると, 5%製剤250mLで7500pg.
血漿量を2500mLと仮定すると, 1本投与にて3pg/mL上昇する計算.
免疫グロブリンとβ-Dグルカン
日本国内で使用可能なIVIG製剤7種で各製剤3ロットずつβ-Dグルカンを測定.
(感染症誌 2017;91:1-6)
・含有量は製剤により差がある
・最も高濃度の300pg/mLを5g(100mL)投与すると
血漿量2500mlでは12pg/mL上昇する計算となる
同じ論文で, IVIG投与前にβ-Dグルカンが陰性であった51例で投与後のβ-Dグルカンを評価
・投与期間は2.9±1.2日, 投与量は15g(2.5~150g, 50mL~3000mL)
・投与前後のβ-Dグルカン:
・使用終了~3日[1-6]で評価され, β-Dグルカン値は有意に上昇を認めた.
>20pg/mLは5/51で認められ, 最も上昇した症例では44.5pg/mL上昇
・上昇例と非上昇例では製剤や投与量, 期間に差は認められない.
透析膜とβ-Dグルカン
Literature reviewでは,
透析膜は, Unmodified cellulose膜でβ-DGが偽陽性となる
Modified celluloseでは結果が割れている.
(Mycoses. 2015 Jan;58(1):4-9. doi: 10.1111/myc.12267.)
・Unmodified celluloseでは, 透析後の数値は平均100pg/mL
・日本からの報告では,Modified cellulose膜を使用した透析において, β-DGが中央値2778pg/mLに上昇した報告がある
日本国内より, 透析前後のβ-Dグルカンを評価した報告
(Kidney International, Vol. 60 (2001), pp. 319–323 )
・β-DグルカンはCellulose膜でのみ顕著に上昇を認める.
Cellulose triacetate, PMMA膜では上昇しない.
-----------------------------
この辺の感覚を踏まえておかないと, ICUで過少・過大評価に繋がるかもしれません.
結構β-Dグルカン値を解釈でこの辺の議論になることが多いです.
実際どの程度これらの因子が影響するのか?
アルブミンとβ-Dグルカン
ICUでβ-DGを評価した267例の後ろ向き解析.
(Eur J Clin Microbiol Infect Dis. 2015 Feb;34(2):357-65. )
・BG試験におけるIFIに対する感度, 特異度を, アルブミン投与, Ig投与, 輸血施行群で評価, 比較
・全体の評価では, カットオフ 95.9pg/mLで, 感度82.9%, 特異度56.7%
・アゾール系抗真菌薬の使用, IVIG, RBC輸血はBG試験の感度, 特異度に影響は認められず.
・アルブミン投与のみ, BG試験の感度, 特異度に影響あり
>30gのAlb(20%製剤で>150mL)を2日以内に投与している場合, BG試験の感度は低下する. 感度36.2%[25.0-48.7], 特異度84.7%[77.5-90.3]
この場合のカットオフは203.7pg/mL
中国における前向きStudy: ICU患者267例において, Alb投与前後のβ-DGを評価.
(Zhonghua Wei Zhong Bing Ji Jiu Yi Xue. 2015 Aug;27(8):672-6. )
・β-DGの変化(ng/L)
IFI否定群では 11.25±2.33 → 10.99±1.07, p=0.085
IFI疑い群 53.14±5.53 → 49.22±8.11, p=0.693
IFI濃厚群 90.30±9.38 → 85.41±10.11, p=0.860
IFI群 100.98±19.24 → 103.21±17.66, p=0.449
アルブミン投与してもβ-Dグルカンの上昇に関連しない報告もあれば, 大量投与により偽陽性が増加する報告もある.
実際アルブミン製剤にどの程度β-Dグルカンが含まれているかを評価した報告もある.
人血清アルブミン5%製剤の国産製品3種類(A-C)と海外製品1種類(D)における含有量を評価
(Therapeutic Research 2013;34:1261-1269)
・β-Dグルカン(pg/mL)
・海外製品の含有量が高いが, 国産製品の含有量は多くはない.
・30pg/mLと仮定すると, 5%製剤250mLで7500pg.
血漿量を2500mLと仮定すると, 1本投与にて3pg/mL上昇する計算.
免疫グロブリンとβ-Dグルカン
日本国内で使用可能なIVIG製剤7種で各製剤3ロットずつβ-Dグルカンを測定.
(感染症誌 2017;91:1-6)
・含有量は製剤により差がある
・最も高濃度の300pg/mLを5g(100mL)投与すると
血漿量2500mlでは12pg/mL上昇する計算となる
同じ論文で, IVIG投与前にβ-Dグルカンが陰性であった51例で投与後のβ-Dグルカンを評価
・投与期間は2.9±1.2日, 投与量は15g(2.5~150g, 50mL~3000mL)
・投与前後のβ-Dグルカン:
・使用終了~3日[1-6]で評価され, β-Dグルカン値は有意に上昇を認めた.
>20pg/mLは5/51で認められ, 最も上昇した症例では44.5pg/mL上昇
・上昇例と非上昇例では製剤や投与量, 期間に差は認められない.
透析膜とβ-Dグルカン
Literature reviewでは,
透析膜は, Unmodified cellulose膜でβ-DGが偽陽性となる
Modified celluloseでは結果が割れている.
(Mycoses. 2015 Jan;58(1):4-9. doi: 10.1111/myc.12267.)
・Unmodified celluloseでは, 透析後の数値は平均100pg/mL
・日本からの報告では,Modified cellulose膜を使用した透析において, β-DGが中央値2778pg/mLに上昇した報告がある
日本国内より, 透析前後のβ-Dグルカンを評価した報告
(Kidney International, Vol. 60 (2001), pp. 319–323 )
・β-DグルカンはCellulose膜でのみ顕著に上昇を認める.
Cellulose triacetate, PMMA膜では上昇しない.
-----------------------------
この辺の感覚を踏まえておかないと, ICUで過少・過大評価に繋がるかもしれません.
結構β-Dグルカン値を解釈でこの辺の議論になることが多いです.